Mycose vaginale récidivante : comment (enfin) en venir à bout ?

Rien n’est plus frustrant pour une femme que de se croire enfin débarrassée d’une mycose vaginale, puis de la voir réapparaître sournoisement quelques semaines plus tard. Ces infections, qu’on pense souvent bénignes et passagères, deviennent pour certaines un véritable fléau récurrent. On parle alors de mycose vaginale récidivante ou, plus largement, de candidose chronique. Si vous vous reconnaissez dans cette situation, sachez que vous êtes loin d'être seule. Environ 8 % des femmes connaissent ce type d’inconfort persistant. Et malheureusement, les traitements classiques – ovules antifongiques, crèmes locales ou médicaments par voie orale – ne suffisent souvent pas à enrayer durablement le problème.
Mais si la clef se trouvait ailleurs ? Et si, pour guérir vraiment, il fallait déplacer notre regard de la muqueuse vaginale vers un autre organe clé : l’intestin. De plus en plus de recherches scientifiques récentes pointent en effet l’existence d’un lien étroit, profond et souvent sous-coté entre le microbiote intestinal et le microbiote vaginal. Ce lien, les chercheurs l’ont baptisé le "gut-vagina axis". Et c’est peut-être cette connexion subtile, médiatrice entre nos différents systèmes, qui pourrait enfin vous aider à retrouver une santé intime stable, confortable et durable.
Le lien entre flore intestinale et flore vaginale : le fameux "gut-vagina axis"
Le "gut-vagina axis" désigne la communication complexe entre l’intestin et le vagin, orchestrée par différents canaux biologiques : immunitaires, hormonaux, inflammatoires, mais aussi anatomiques. En clair, notre flore intestinale influence en profondeur l’équilibre de notre flore vaginale. Ce n’est pas une image, c’est une réalité biologique observable.
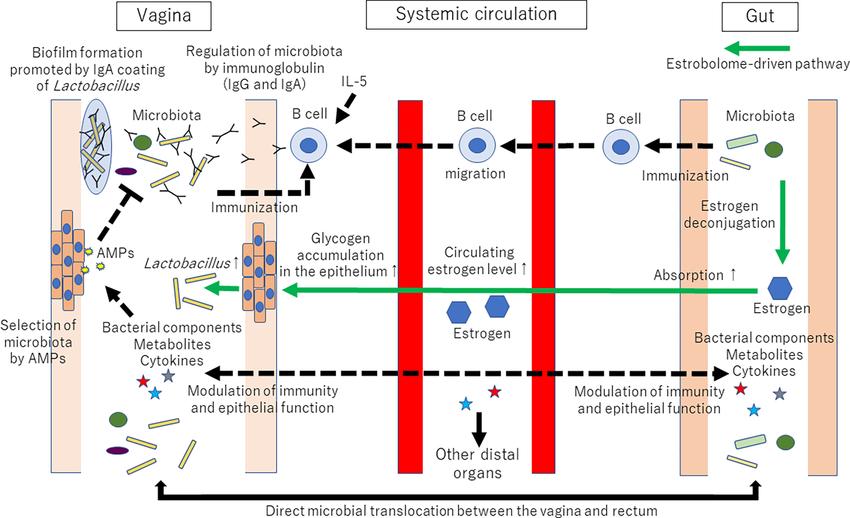
D’abord, sur le plan anatomique, le vagin et le rectum sont voisins. Cette proximité favorise les transferts bactériens et fongiques d’une zone à l’autre, notamment chez les femmes. Des études ont mis en évidence la présence de certaines souches de Candida à la fois dans le microbiote intestinal et vaginal, suggérant une migration directe entre ces deux territoires.
Ensuite, le microbiote intestinal joue un rôle majeur dans la régulation du système immunitaire. Une flore intestinale perturbée (ou "dysbiose") peut entraîner une réponse inflammatoire exagérée ou inefficace, y compris dans la sphère vaginale. En clair, si l’intestin est déséquilibré, l’organisme aura plus de mal à se défendre contre les infections vaginales, notamment celles liées à Candida albicans.
Le troisième lien se trouve du côté hormonal. Certaines bactéries intestinales participent activement au métabolisme des œstrogènes via ce qu’on appelle l’estrobolome. Quand cet ensemble de bactéries est déséquilibré, cela peut engendrer une dominance œstrogénique, c’est-à-dire un excès relatif d’œstrogènes non éliminés. Or, on sait que des taux élevés d’œstrogènes favorisent l’adhérence et la croissance du Candida au niveau vaginal.
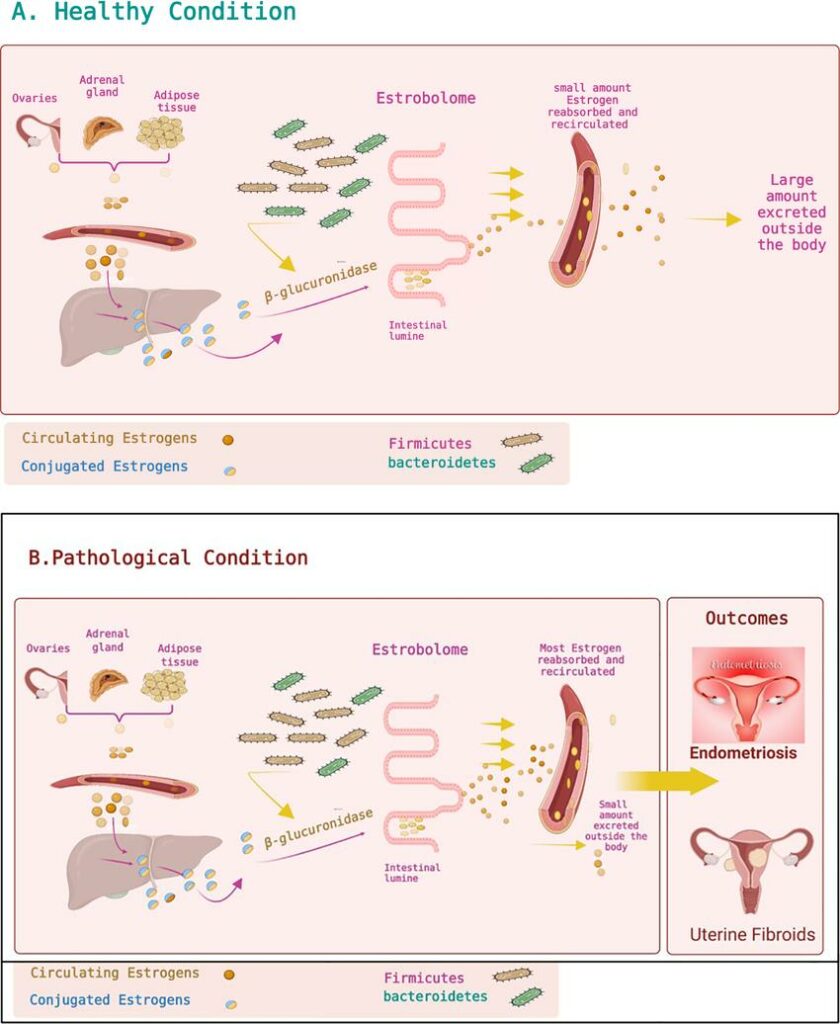
Enfin, une dysbiose intestinale chronique peut engendrer une inflammation systémique, notamment via le phénomène d'hyperperméabilité intestinale (leaky gut). Ce terrain inflammatoire chronique entretient un climat favorable aux infections répétées et affaiblit les capacités de régénération des muqueuses.
Comprendre ces interactions, c’est ouvrir les yeux sur le fait que la santé intime féminine ne se résume pas à l’usage d’un ovule antifongique, mais exige une vision systémique et écologique du corps.
Les causes profondes d’une mycose vaginale récidivante : au-delà des apparences
Derrière une mycose vaginale qui récidive se cachent souvent des causes sous-jacentes qu’il est essentiel d’éclairer. L’une des premières que j’observe en cabinet est le stress chronique. Celui-ci impacte négativement l’axe intestin-cerveau, modifie la composition du microbiote intestinal et affaiblit l’immunité. Cela crée un terrain idéal pour que Candida prolifère.
Une autre cause fréquente est la fameuse dominance œstrogénique. Ce déséquilibre hormonal, que l’on retrouve souvent en cas de syndrome prémenstruel, d’endométriose ou suite à une contraception hormonale, crée un milieu favorable à la candidose. Candida albicans adore les œstrogènes !
Il faut également mentionner la toxicité du cuivre, que l’on retrouve parfois en excès dans l’organisme (notamment chez les femmes portant un stérilet au cuivre ou ayant pris la pilule contraceptive). Ce métal perturbe les fonctions immunitaires et peut favoriser la persistance des infections fongiques.
Les antibiotiques constituent eux aussi un facteur clé. En altérant la flore intestinale et vaginale, ils suppriment les bactéries protectrices (notamment les Lactobacilles) qui maintiennent Candida sous contrôle. Sans ces alliées, la voie est libre pour la prolifération fongique.
Il faut aussi évoquer les métaux lourds, en particulier le mercure. Ce dernier perturbe fortement le système immunitaire, favorise l’inflammation chronique, et altère l’équilibre du microbiote. Un terrain idéal pour une candidose chronique.
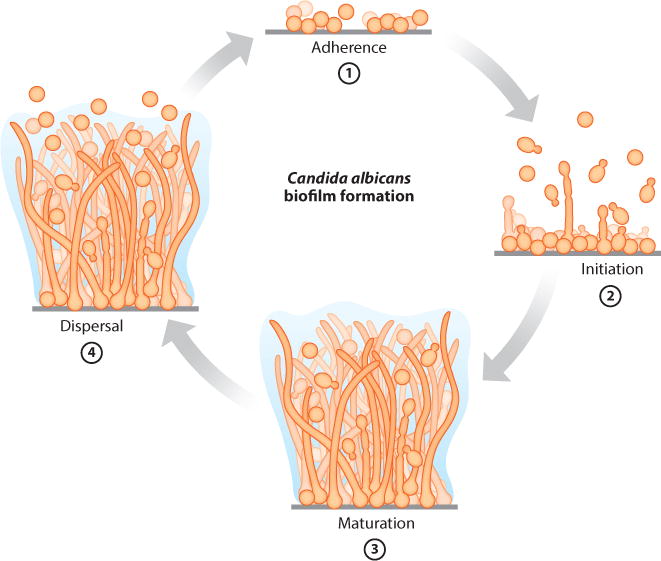
Enfin, les biofilms représentent un obstacle redoutable : il s’agit de structures protectrices formées par le Candida lui-même pour se cacher du système immunitaire et résister aux traitements antifongiques. Ce "bouclier" rend la mycose bien plus difficile à déloger.
Comment se débarrasser durablement d’une mycose vaginale ?
À cette question, je réponds toujours avec sincérité : seule une approche personnalisée et accompagnée peut apporter une solution durable. Lorsque la mycose revient, malgré l’emploi d’ovules, d’huiles essentielles ou de probiotiques en automédication, c’est qu’il est temps de prendre du recul et de se faire guider. Car oui, chaque femme est unique, et chaque candidose a sa propre racine.
Il m’arrive très fréquemment d’accueillir en consultation des femmes ayant testé mille et une solutions glanées sur Internet. Des protocoles tout faits, parfois contradictoires, souvent incomplets. Mais la vérité, c’est que le traitement efficace est toujours individualisé. Il prend en compte le terrain de la personne, ses analyses biologiques, son mode de vie, son histoire hormonale, digestive, émotionnelle.
Travailler sur la candidose, c’est travailler sur soi, en profondeur. C’est comprendre que l’objectif n’est pas seulement détruire un champignon, mais de restaurer un équilibre écologique global. Cela implique souvent de reconstruire le microbiote intestinal, de réguler les hormones, de soutenir le foie et les émonctoires, de réparer les muqueuses, de lever les blocages émotionnels. Et tout cela prend du temps. Comptez plusieurs mois, parfois davantage.
Quant aux antifongiques chimiques, ils peuvent offrir un soulagement temporaire, mais sans travail de fond, la récidive est fréquente. Je le vois chez de nombreuses patientes qui, après plusieurs cycles de traitements médicaux, n’ont pas vu de résultat durable.
Conclusion
Il est temps de déconstruire l’idée selon laquelle une mycose vaginale n’est qu’un petit dérèglement local et sans conséquence. Lorsqu’elle devient récidivante, elle est le témoin d’un déséquilibre plus profond, systémique, intime.
En explorant les causes racines – qu’elles soient intestinales, hormonales, environnementales ou émotionnelles – et en adoptant une démarche globale et adaptée, il est tout à fait possible de retrouver une santé intime durable. Et avec elle, la sérénité, la confiance, et le soulagement profond que beaucoup de femmes attendent depuis des années.
Sources :
Drell, T., Lillsaar, T., Simm, J., Aasp\u00f5llu, A., Vain, E., S\u00e4rekanno, E., ... & Metsis, M. (2013). Comparison of microbial populations in vaginal, rectal and perineal samples from pregnant women. FEMS Microbiology Ecology, 83(2), 556-565. https://doi.org/10.1111/1574-6941.12117
Li, X., Chen, J., Sun, Y., & Li, Y. (2023). Female reproductive tract-organ axes: A comprehensive review of the gut-vagina axis, gut-uterus axis, and gut-ovary axis. Frontiers in Endocrinology, 14, 1126345. https://doi.org/10.3389/fendo.2023.1126345
Plottel, C. S., & Blaser, M. J. (2011). Microbial endocrinology: the microbiota and the estrobolome. Science Translational Medicine, 3(77), 77ps12. https://doi.org/10.1126/scitranslmed.3002701
Sobel, J. D. (2007). Vulvovaginal candidosis. The Lancet, 369(9577), 1961-1971. https://doi.org/10.1016/S0140-6736(07)60917-9
O'Mahony, S. M., Clarke, G., Borre, Y., Dinan, T. G., & Cryan, J. F. (2015). The microbiome and childhood diseases: Focus on brain-gut axis. Birth Defects Research Part C: Embryo Today: Reviews, 105(4), 296-313.
Kwa, M., Plottel, C. S., Blaser, M. J., & Adams, S. (2016). The Intestinal Microbiome and Estrogen Receptor–Positive Female Cancers. Journal of the National Cancer Institute, 108(8), djw029. https://doi.org/10.1093/jnci/djw029https://doi.org/10.1002/bdrc.21115
Brewer, G. J. (2010). Copper toxicity in the general population. Clinical Neurophysiology, 121(4), 459-460. https://doi.org/10.1016/j.clinph.2009.11.072
Pizzorno, J., Murray, M. T., & Joiner-Bey, H. (2011). The toxic effects of mercury and its influence on chronic diseases. Integrative Medicine: A Clinician's Journal, 10(3), 42.
Nobile, C. J., & Johnson, A. D. (2015). Candida albicans biofilms and human disease. Annual Review of Microbiology, 69, 71-92. https://doi.org/10.1146/annurev-micro-091014-104330
A PROPOS

Estelle Castellanos
Diététicienne-nutritionniste DE
Naturopathe
Fondatrice de la plateforme ATAVI
Santé fonctionnelle
FBCS
Spécialiste des maladies liées aux moisissures
Mycothérapeute certifiée

